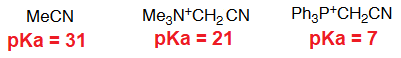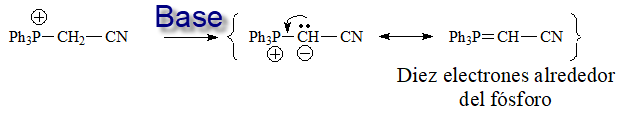ADICIÓN DE NUCLEÓFILOS DE CARBONO A ALDEHÍDOS Y CETONAS
Esta es una reacción muy importante porque permite la formación de enlaces C-C y aumentar la complejidad de la molécula producto.
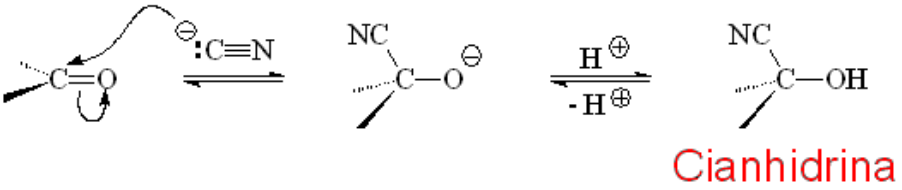
El nucleófilo de carbono quizá más simple que existe, el cianuro, reacciona con aldehídos y cetonas para dar un nuevo compuesto: una cianhidrina.
La reacción es muy simple y útil ya que el grupo CN puede convertirse en otros grupos funcionales.
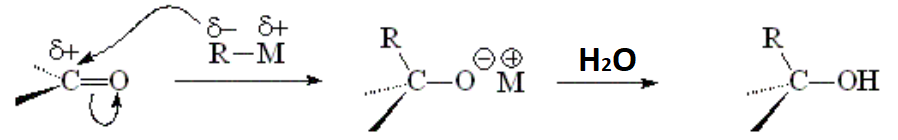
ORGANOMETÁLICOS DE LITIO Y MAGNESIO (GRIGNARD)
Dependiendo de que usemos el formaldehído, un aldehído o una cetona obtendremos un alcohol primario, secundario o terciario, respectivamente.
IMPORTANTE: Hay numerosas funciones que compiten o que simplemente destruyen el organometálico, como los alcoholes, aminas y ácidos carboxílicos entre muchas otras.
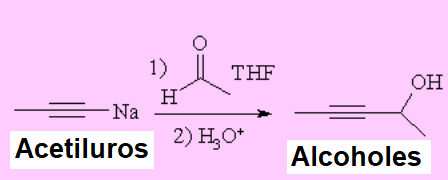
Los alquinuros, obtenidos por acción de una base fuerte sobre un alquino terminal, son excelentes nucleófilos, que pueden dar fácilmente adiciones a grupos carbonilo.
IMPORTANTE: Hay numerosas funciones que compiten o que simplemente destruyen el alquinuro, como los alcoholes, aminas y ácidos carboxílicos entre muchas otras.
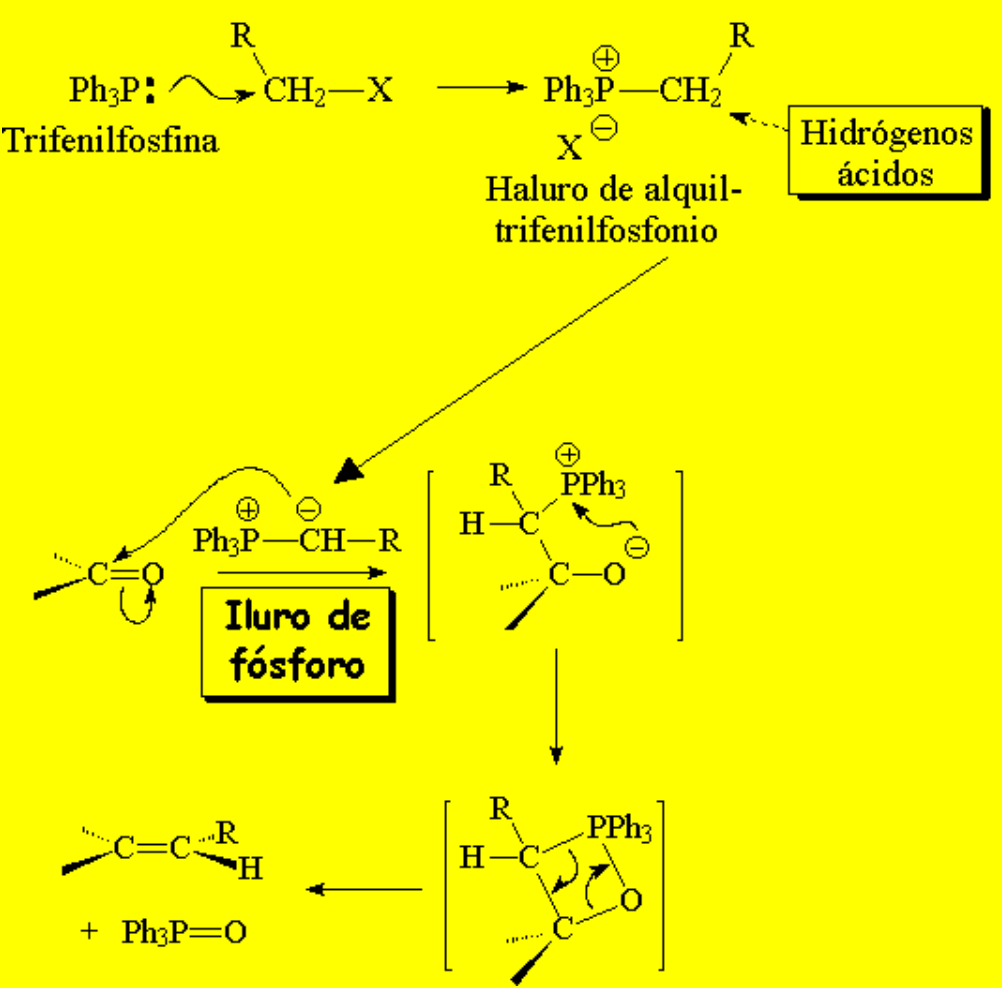
Esta reacción ya se ha mencionado en el capítulo de alquenos ya que se utiliza para su preparación.
El compuesto clave en este proceso es el iluro de fósforo, que se forma gracias a que los hidrógenos contiguos a una sal de fosfonio tienen una cierta acidez.
Esto diferencia a las sales de fosfonio de las de amonio.
¿Qué provoca esa acidez de las sales de fosfonio?
La única manera de explicar que la sal de fosfonio tenga una acidez tan alta es que el fósforo puede habilitar orbitales 3d para deslocalizar la carga negativa del iluro formado.
¡El nitrógeno no puede!