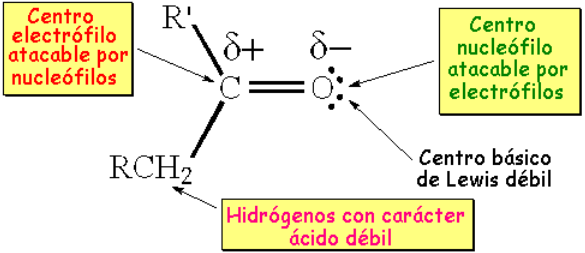
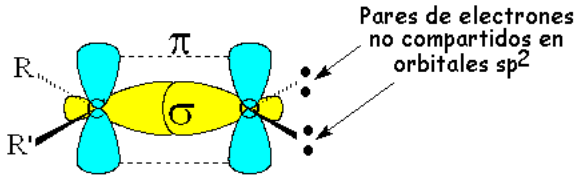
Los ángulos y distancias de enlace medidos experimentalmente son compatibles con una hibridación sp2 de los átomos que forman el enlace C=O.
La forma resonante con separación de cargas explica la deficiencia electrónica que el carbono tiene en un enlace C=O. Esta es una diferencia importante con el enlace C=C.
La mayor electronegatividad del oxígeno provoca una polarización del enlace C=O que marca su reactividad y, muy IMPORTANTE, la de su posición adyacente.
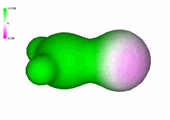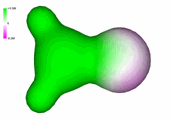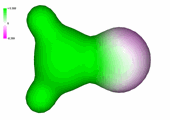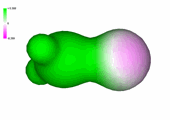 Densidad de carga en el formaldehído
Densidad de carga en el formaldehído
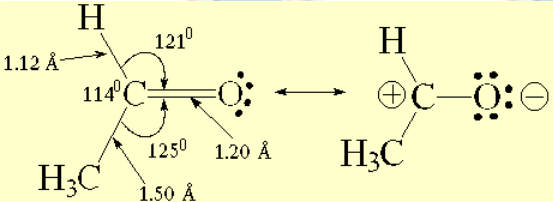 Parámetros estructurales del acetaldehído
Parámetros estructurales del acetaldehído