LA FORMA DE LAS SEÑALES
(ACOPLAMIENTOS)
Ya has visto ejemplos de multipletes.
Cuando un grupo de hidrógenos equivalentes dan un “N-plete” es que tienen “N-1” hidrógenos vecinos.
¿Lo entiendes?
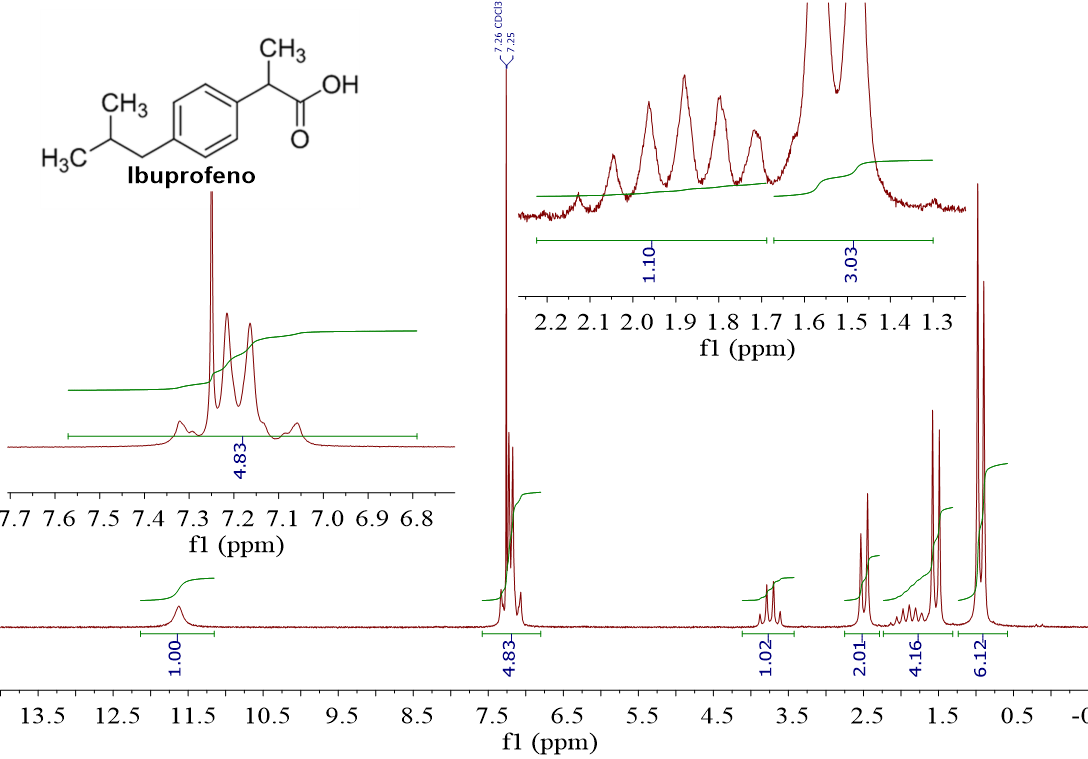
Te he hecho trampa porque hasta ahora eso lo hemos visto del revés: un grupo de hidrógenos vecinos a un grupo de “N” hidrógenos ocasiona en estos últimos un “N+1-plete”. El ibuprofeno es un excelente ejemplo:
La señal “mas apantallada” (0.9 ppm) integra para 6 y es un “doblete”, es decir, son 6 hidrógenos equivalentes vecinos a uno sólo. En la estructura, los dos grupos CH3 de la izquierda cumplen estas condiciones.
La siguiente señal (1.5 ppm) integra para 3 (mira la ampliación dentro del espectro) y es un “doblete”, es decir, son 3 hidrógenos equivalentes vecinos a uno sólo. En la estructura, el grupo CH3 de la parte superior cumple estas condiciones.
La siguiente señal (1.5-2.1 ppm) es muy compleja y está parcialmente “solapada” con el doblete a 1.5 ppm. La dejaremos para más tarde.
A continuación viene la señal a 2.5 ppm que integra para 2 y es un “doblete”, es decir, dos hidrógenos equivalentes vecinos a uno sólo. Estas condiciones sólo las cumple el único grupo CH2 de la molécula, que es vecino a un grupo CH.
A 3.7 ppm hay una señal que integra para 1 y es un “cuartete”, es decir, un protón que es vecino a tres. Eso sólo lo cumple el grupo CH de la parte superior de la estructura.
Después hay una señal compleja (7.2 ppm) que casi integra para 5. Por el desplazamiento químico tan desapantallado, esta señal sólo puede corresponder a los 4 hidrógenos aromáticos. Pero, ¡cuidado!
En la ampliación se ve que hay una señal más alta y más fina que sale a 7.26 ppm y que corresponde al disolvente CDCl3. Su aportación a la integral “falsea” el valor esperado de 4 para los hidrógenos aromáticos. La “forma” o “multiplicidad” de estas señales es compleja porque la simetría del anillo es tal que los 4 hidrógenos son solo equivalentes por parejas y cada pareja “resuena” a desplazamientos químicos muy parecidos (7.10 ppm y 7.25 ppm, aproximadamente).
La última señal aparece a un desplazamiento químico extraordinariamente alto y “desapantallado”. Sólo nos queda por asignar el H del grupo OH y el H del CH de la parte izquierda. El primero no tiene vecinos al estar unido al grupo COO, así que debe ser éste. ¿Cuántos vecinos tiene el grupo CH que nos queda por entender? Pues 6 hidrógenos de los grupos CH3 y 2 del grupo CH2, es decir 8 hidrógenos, lo que hace que tenga que salir como un multiplete de 8+1 “patas”. Desgraciadamente no se ven todas porque el doblete a 1.5 ppm se solapa.
¿Por qué las señales de los protones que tienen “vecinos” se desdoblan y aparecen como multipletes?
En los enlaces siguientes encontrarás las respuestas...